 |
Справочник минералов |
Минералогия | Геология | Жизнь в поле |
Интересные ссылки |
О сайте |  |
|
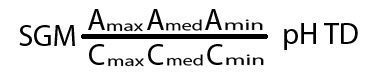
Грамм-эквивалент - масса вещества в граммах, умноженную на молярную массу вещества.
Процент-эквивалент - вычисляется путём деления грамм-эквивалента вещества на сумму всех грамм-эквивалентов веществ смеси (в данном случае - анинов ИЛИ катионов) и умножением на 100%.
Формула читается (см. пример): гирокарбонатно-сульфатно-хлоридная кальциево-натриево-магниевая вода.
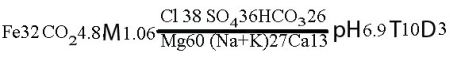
Формула солевого состава - формула Курлова, где указываются ионы, содержание которых более 10 %-экв.
Агрессивность воды - разрушающее действие воды на строительные материалы подземной части сооружения.
Жёсткость воды определяется содержанием ионов Ca и Mg (посмотреть ГОСТ).
| Жёсткость воды. | |
|---|---|
| Общая (Сумма ионов Ca и Mg). | Устранимая (говоря проще, накипь). |
| Неустранимая (остаётся после кипячения). | |
PS: Лучшее средство от накипи - фанта. Заливаешь на полчасика, и никаких проблем. Задумайся!
Солёность воды - содержание в воде хлоридов и сульфатов Na, Mg, Ca (посмотреть ГОСТ).
| Классификация вод по солёности (по А.М. Овчинникову). | |||
|---|---|---|---|
| Тип солёности. | Класс солёности. | Минерализация, г/л. | Химический тип. |
| Пресные. | Ультрапресные. | < 0.2 | Обычно - гидрокарбонатные. |
| Пресные. | 0.2 - 0.5 | ||
| Воды с относительно повышенной минерализацией. | 0.5 - 1 | Гидрокарбонатно-сульфатные. | |
| Солоноватые. | Солоноватые. | 1 - 3 | Сульфатно-хлоридные. |
| Солёные. | Солёные. | 3 - 10 | Преимущественно - хлоридные. |
| Воды повышенной солёности. | 10 - 35 | ||
| Рассолы. | Воды, переходные к рассолам. | 35 - 50 | Хлоридные. |
| Рассолы. | 50 - 400 | ||
| Ессентуки №17; скв. № 47 | |
|---|---|
| CO3 | 5300 - 6500 |
| SO4 | < 25 |
| Cl | 1200 - 2200 |
| Ca | < 100 |
| Mg | < 100 |
| K+Na | 2700 - 3700 |
| HBO3 | 35 - 80 |
| M | 9.2 - 12.7 |
| Нарзан. скв 5/0, 5/0-бис, 7-РЭ | |
|---|---|
| HCO3 | 1000 - 1500 |
| SO4 | 300 - 500 |
| Ca | 300 - 400 |
| Mg | 80 - 120 |
| K+Na | 130 - 200 |
| M | 2 - 3 |
| Сенежская. скв 1/ГВК46240620, 2/ГВК46219780 | |
|---|---|
| HCO3 | 400 |
| F | 1.2 |
| I | 12.5 |
| Ca | 100 |
| Mg | 80 - 120 |
| K+Na | 220 |
| M | 0.5 |
| Жёсткость | 7 мг-экв/л |
| Щелочность | 6.5 мг-экв/л |
| Боржоми лайт. скв. 38, ист Даба | |
|---|---|
| HCO3 | 1000-1400 |
| SO4 | < 15 |
| Ca | 25 - 50 |
| Cl | 80 - 120 |
| F | 2 - 4 |
| I | 0.1-0.3 |
| Ca | 25 - 50 |
| Mg | < 25 |
| K+Na | 355 - 510 |
| M | 1.5 - 2 |
| Ионы и их свойства. | |||
|---|---|---|---|
| Тип ионов. | Ионы. | Заряд. | Молярная масса. |
| Кислотные остатки. | SO4 | 2- | 96.06 |
| HBO3 | 2- | 59.816 | |
| CO3 | 2- | 60.008 | |
| HCO3 | - | 61.016 | |
| Галогены. | Cl | - | 35.008 |
| F | - | 10.998 | |
| Br | - | 79.904 | |
| I | - | 126.905 | |
| Щелочные металлы. | Ca | 2+ | 40.08 |
| Mg | 2+ | 34.312 | |
| NaK | 2+ | 62.092 | |